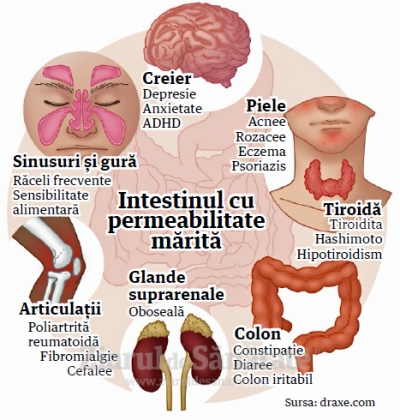
Despre rolul nutriției, al terenului biologic și al tipului metabolic tumoral în definirea terapiei personalizate
Ziarul de Sănătate continuă seria interviurilor cu renumitul Prof. John Ionescu (Germania), biolog și imunolog de excepție, cu o temă de actualitate: abordarea integrativă a bolilor neoplazice. În ciuda evoluției medicinei, boala neoplazică este una dintre principalele cauze de deces la nivel mondial. Distinsul Prof. John Ionescu ne dezvăluie „biologia“ cancerului, ne explică rolul toxinelor, al nutriției și terenului biologic în abordarea bolilor neoplazice. Pe 19 martie 2016, Prof. John Ionescu revine la București pentru cel de-al doilea Seminar de Medicină Integrativă de anul acesta, a cărui temă va fi chiar „Abordarea integrativă a bolilor neoplazice“.
Ziarul de Sănătate: Cum se definește boala neoplazică? Care sunt cele mai frecvente tipuri de cancer?
Prof. John Ionescu: Putem considera boala neoplazică drept cea mai gravă maladie a secolului XXI, aflată într-o fulminantă expansiune. La baza acestei maladii stă interacțiunea dintre genomul uman și o serie întreagă de factori nocivi din mediul înconjurător, aflați și ei într-o creștere rapidă în ultimele 6 decenii. Fără a enumera aici cele mai importante caracteristici ale metabolismului tumoral, amintesc că în urma interacțiunii dintre genomul uman și factorii de mediu menționați mai sus, se ajunge la pierderea controlului multiplicării celulare în cadrul unui țesut sau altuia și la pierderea controlului imunitar asupra acestor celule modificate. Ca atare, creșterea tumorală, pe care o putem asemăna cu o creștere embrionară prin caracterul ancestral al acestor celule, avansează în mod autarhic, necontrolat, conducând la distrugerea organelor și a funcțiilor respective. Multiplicarea celulară malignă poate afecta, în principiu, toate organele, cu mici excepții, cum ar fi mușchiul cardiac, iar tumorile respective pot fi împărțite, în mod artificial, în tumori solide și leucemii (multiplicări necontrolate ale celulelor seriei albe sangvine).
ZDS: Este cancerul o maladie a societății moderne? În ce măsură putem spune că boala canceroasă este o boală de mediu?
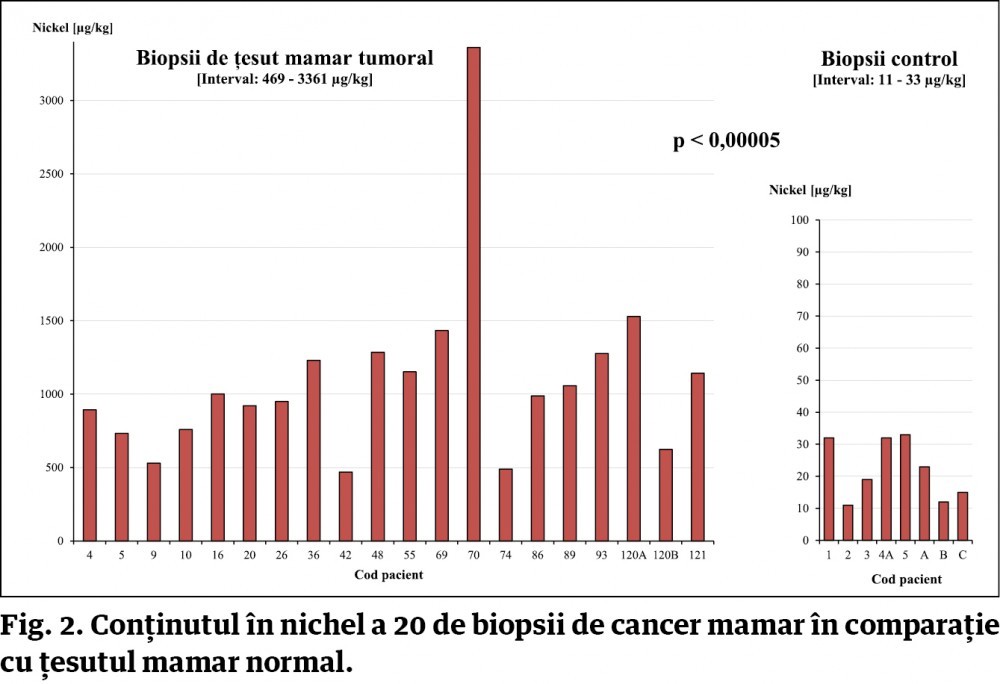
Prof. John Ionescu: Cu siguranță, evoluția bolii canceroase se asociază cu creșterea masivă a poluării mediului, dar și cu avansarea în vârstă. Frecvența acestei maladii este mult mai scăzută în secolele XIX-XX și arată o creștere aproape exponențială în a doua jumătate a secolului XX. Dovada rolului jucat de mediul înconjurător o aduce și cantitatea enormă de toxine organice și metale grele, pe care le găsim acumulate tocmai în structura tumorilor maligne.
ZDS: Care sunt categoriile de persoane cele mai afectate de poluare?
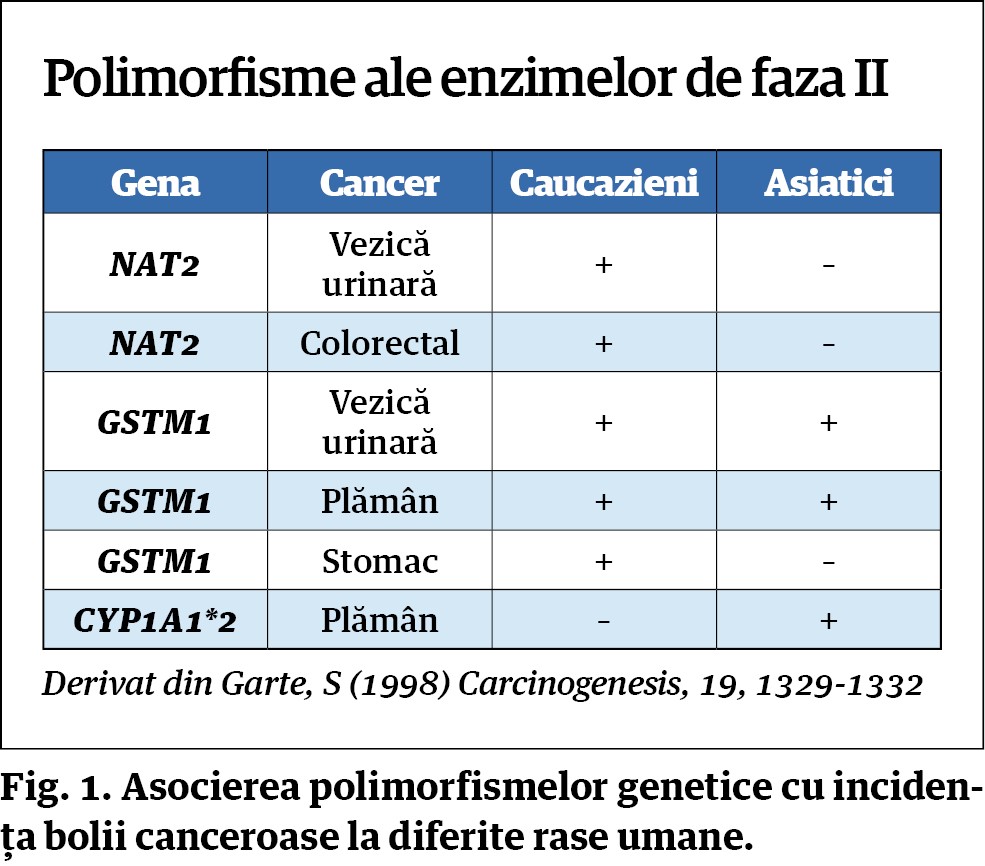
Prof. John Ionescu: Poluarea ne afectează pe toți, fără îndoială, contribuind în mod direct la reducerea eficienței sistemului imun și la creșterea susceptibilității la infecții virale și microbiene. Mai sensibile și mai expuse la a face boala canceroasă sunt însă persoanele care din cauza polimorfismelor genetice, pe care le putem dovedi prin teste de expresie genetică, nu sunt capabile să metabolizeze, să dezintoxice și să elimine substanțele chimice cu care vin în contact. Deosebim astfel persoane incapabile să dezintoxice metalele grele, marcate prin polimorfisme ale enzimelor de faza II (GSTM1, GSTP1, NAT2, UGT, sulfotransferaze), sau persoane care nu pot metaboliza diferite medicamente prin polimorfismele de faza I (CYP450).
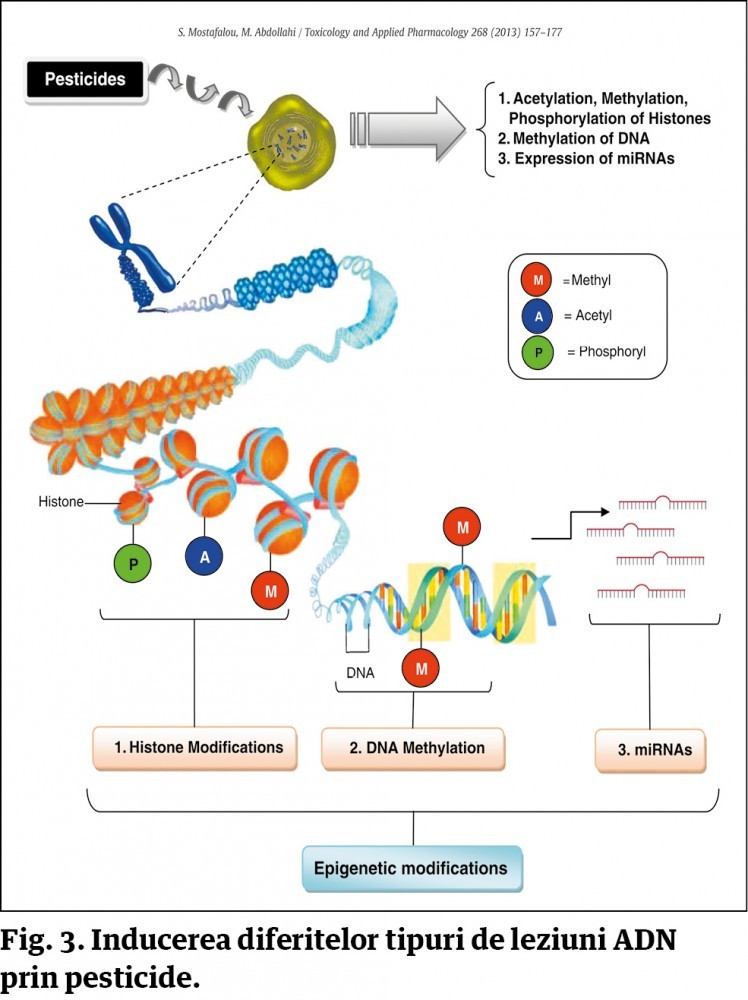
Susceptibilitatea genetică a acestor persoane le conferă o capacitate mult mai crescută de a acumula organo-toxinele și metalele grele, pe care ulterior le găsim fără excepție în structura tumorilor maligne din corp. Aceste polimorfisme genetice există de mii de ani, lipsa substanțelor toxice a făcut ca prezența maladiei canceroase să fie nesemnificativă până în secolul XX. Până la acea vreme nu existau aliajele dentare, nu existau aditivii alimentari, detergenții, vopselele industriale, impregnarea covoarelor, utilizarea ierbicidelor, pesticidelor și organofosfaților în agricultură ș.a.m.d.
ZDS: Unii doctori spun că un cancer se poate dezvolta latent chiar și în 5-10 de ani. Aceasta înseamnă că au fost irosiți 5-10 de ani în care s-ar fi putut interveni de timpuriu. Ce s-ar fi putut face pentru o detectare foarte timpurie a bolii respective?
Prof. John Ionescu: Într-adevăr, unele forme de cancer arată o dezvoltare lentă pe parcursul mai multor ani. Ceea ce se poate face deosebit de timpuriu pentru depistarea predispoziției la o boală canceroasă este tocmai investigarea polimorfismelor genetice la aceste persoane, care chiar de la naștere pot arăta în ce măsură oncogenele persoanei respective o predispun la un cancer mamar (asocierea cu oncogenele BRCA1/2), la un cancer de colon (asocierea cu oncogenele APC, MLH1, MSH2) sau la leucemie (asocierea cu mutații ale supresorului tumoral TP53). Deosebit de importante în aprecierea riscului sunt și polimorfismele enzimelor de detoxifiere ale organismului (Fig. 1), care pot indica de timpuriu incapacitatea organismului în metabolizarea și eliminarea substanțelor poluante din mediul înconjurător. Pe lângă aceste polimorfisme genetice, biologia moleculară din ultimele decenii mai oferă o serie de teste de imunologie și biochimie medicală, care pot să deceleze timpuriu modificări semnificative ale aparatului enzimatic (TKTL1, M2PK, tirozin kinaza, izoenzime LDH, PDK1, aromataza) și markeri structurali din membranele celulelor maligne, așa-numiții markeri tumorali (CA12-5, CA19-9, CA15-3, CEA etc.), care pot fi determinați încă înainte ca tumorile respective să poată fi detectate prin metode de imagistică. Acești markeri tumorali, care se detectează în serul pacientului, îți arată creșteri chiar în situația în care organul se află într-o stare de inflamație benignă. Putem astfel afla că pacientul este la risc înainte să apară tumora. Din păcate, acești markeri nu sunt 100% specifici pentru o tumoră a unui organ, din cauza variabilității genetice a celulelor tumorale.
ZDS: În ce măsură pot fi prevenite bolile neoplazice?
Prof. John Ionescu: Având în vedere cauzele menționate mai sus care pot duce la apariția unei boli neoplazice, consider că factorii principali în profilaxia tumorilor canceroase sunt gradul de poluare a mediului înconjurător și hrana pe care o ingerăm zi de zi. Este cunoscut atât faptul că poluarea chimică din locuință sau de la locul de muncă, diverse intervenții medicale (de genul protezelor metalice și al aliajelor dentare), asociate cu o hrană necorespunzătoare, incluzând un exces cronic de carbohidrați simpli cu indice glicemic crescut sau cu un consum deosebit de crescut de carne roșie (vită, porc, vânat), pe lângă alte obiceiuri, precum fumatul, consumul de alcool sau droguri, pot iniția și accelera o evoluție neoplazică. Bineînțeles că mai sunt și alți factori legați de modul de viață, precum sedentarismul, care poate fi una dintre cauzele principale ale accelerării unor asemenea procese, din cauza oxidărilor celulare scăzute și consumului scăzut de oxigen. Amintesc de asemenea și infecțiile cronice virale (HPV, HTLV, KSHV), bacteriene sau micotice, ce conduc și ele în timp la instalarea unei stări de inflamație cronică asociată cu un shift imunitar Th1->Th2.
ZDS: Ce substanțe găsiți în biopsiile tumorilor pe care le analizați? Sunt cumva tumorile o modalitate a organismului de a scăpa de toxicitatea din corp?
Prof. John Ionescu: Cercetările făcute în ultimul deceniu în laboratoarele noastre din Germania arată o încărcare masivă a tumorilor maligne cu metale tranziționale (fier, nichel, crom, cositor, mercur, cadmiu și, în mod surprinzător, zinc), atingând niveluri de zeci de ori mai mari decât în celulele normale. Spuneam despre zinc că poate părea surprinzător, însă administrarea acestui element unui pacient cu cancer este total contraindicată, ținând cont de faptul că tumora are nevoie de zinc pentru creștere și multiplicare. Pe lângă aceste metale tranziționale, tumorile maligne pot acumula și organo-toxine (de genul pesticidelor, solvenților, vopselelor și substanțelor din fumul de țigară), care contribuie alături de metalele amintite, prin radicalii liberi generați in situ la lezarea ADN-ului celular, producând mutații genetice în mod repetat, ceea ce explică heterogenicitatea și variabilitatea genetică enormă a celulelor canceroase chiar în interiorul aceleiași tumori. Această variabilitate genetică extraordinară asociată cu un exces intracelular de elemente puternic reducătoare (GSH, NADH, cisteină, glucoză etc.), indus de aceleași xenobiotice, explică rezistența tumorilor maligne la tratamentele radioterapeutice și chimioterapeutice aplicate. Din acest motiv, chemoterapia respectivă poate afecta una sau alta dintre populațiile de celule tumorale din acea tumoră, dar nu pe toate. Ca atare, cele care au rezistat acestui atac, datorită variabilității genetice și redozei intracelulare, se vor multiplica mai departe și vor putea metastaza.
În privința celei de-a doua părți a întrebării, putem considera tumorile ca locații de acumulare a toxinelor din mediul înconjurător din cauza imposibilității corpului de a metaboliza, neutraliza și elimina aceste toxine. Depozitele primare de substanțe toxice organice le găsim în țesutul adipos, numai că țesutul adipos nu are capacitate nici de creștere tumorală, nici de metastazare, ci reprezintă un loc de depunere și de izolare a unei părți din substanțele nocive din mediul înconjurător, pe care corpul nu poate să le elimine pe cale renală (prin urină) sau biliară (prin scaun). Ceea ce se depune în țesuturi și organe producând tumorile sunt surplusuri de substanțe nocive pe care corpul nu reușește să le elimine.
ZDS: Care este rolul radicalilor liberi în afectarea ADN-ului celular și în apariția cancerului? Care sunt cele mai importante surse de radicali liberi?
Prof. John Ionescu: După cum am precizat, celulele tumorale acumulează o cantitate imensă de organo-toxine și metale tranziționale. Ambele tipuri de substanțe nocive își exercită influența nefastă asupra ADN-ului celular prin generarea unui exces de radicali liberi ai oxigenului și azotului la nivel celular. Acești radicali liberi agresează materialul genetic celular, producând mutațiile punctuale sau de catenă ADN (rupere de catenă), cunoscute în biologia celulelor tumorale. Aceste mutații conferă heterogenitatea imensă de care am vorbit anterior, deci variabilitatea genetică a acestor celule tumorale, care le permite diverselor populații de celule tumorale din cadrul aceleiași tumori să reziste atacului chemoterapeutic din exterior. Așadar, radicalii liberi au un rol primordial în heterogenicitatea genetică a celulelor tumorale datorită unei agresivități extraordinare atât asupra proteinelor celulare, lipidelor de membrană și, în special, asupra materialului genetic. Sursa principală de radicali liberi ai oxigenului și azotului (superoxid, radical hidroxil, peroxinitrit ș.a.) o constituie organotoxinele și în special metalele tranziționale care, după cum am văzut, generează acești radicali prin reacții chimice de genul Haber-Weiss și Fenton.
ZDS: Ce rol joacă aceste elemente în perturbarea proceselor neuroendocrine în corpul uman?
Prof. John Ionescu: O parte din metalele acumulate în tumori, cum ar fi nichelul si cadmiul, joacă rolul așa-zișilor „endocrine disruptors“, activând receptorii hormonilor estrogeni și inducând semnalele caracteristice la nivel nuclear și, implicit, proliferarea celulară. Tot aceste metale pot altera și raportul metaboliților estrogenici cu scăderea severă a raportului 2-OH/16-OH estrogenilor, măsurat în mod frecvent în urina purtătoarelor de tumori ovariene, mamare și de col uterin. Restabilirea raportului corect al metaboliților menționați (2-OH/16-OH) printr-o serie de suplimente alimentare pe care îi prezentăm la curs se asociază cu o evoluție clinică deosebit de favorabilă.
ZDS: Ce rol credeți că poate avea microbiomul intestinal în dezvoltarea bolii canceroase? Dar inflamația sistemică cronică?
Prof. John Ionescu: Microbiomul intestinal joacă un rol determinant din primele luni de viață, dirijând antrenamentul celulelor imunitare din structurile limfatice asociate tubului digestiv (GALT) în direcția unui răspuns imun stabil, de tip TH1. În cazul unei flore microbiene dereglate la nou-născut, constatăm perpetuarea reacției imunologice de tip fetal (TH2), caracteristică milioanelor de cazuri de boli alergice, apărute în primele 6 luni de viață. Aceeași reacție de tip TH2 o regăsim la copiii care dezvoltă o boală malignă și la adulții cu patologie alergică sau tumorală. Compoziția microbiomului joacă un rol fundamental în antrenamentul sistemului imunitar, respectiv în orientarea acestuia în direcția bună sau greșită. De aceea, atât în cazul copiilor cu boli alergice, de genul astmului și neurodermitei, care intră în tratamentul nostru, cât și în cazul adulților cu boli degenerative sau boli maligne, investigăm cu mare atenție microbiomul intestinal și depunem un efort deosebit în restructurarea acestuia, în sensul reimplantării culturilor fiziologice cu bacterii lactice și eubacterii.
ZDS: Care sunt particularitățile metabolice, funcționale, energetice ale celulelor neoplazice de care trebuie să se țină cont în abordarea terapeutică?
Prof. John Ionescu: Răspunsul corect, și mult mai complet la această întrebare, îl dau în câteva ore în timpul cursului privind abordarea integrativă a tumorilor maligne din 19.03 a.c., în care una dintre temele principale o reprezintă tocmai particularitățile metabolice, funcționale și energetice ale celulelor tumorale.
Ceea ce nu se ia în considerare, din păcate, în abordarea clasică a biologiei tumorale este tocmai importanța eminentă a dezechilibrului acido-bazic dintre interiorul tumorii maligne – care este alcalin – și exteriorul tumorii maligne – care este acid. Această aciditate este întreținută secundă de secundă în toate tumorile maligne prin exportarea în mediul extracelular a protonilor de hidrogen (H+) și a acidului l-lactic, produs final al glicolizei aerobe din celulele tumorale. Acest dezechilibru este strâns legat și de dezechilibrul redox pe care îl constatăm la interiorul și la exteriorul celulei tumorale, în sensul unei redoze intracelulare asociată pH-ului alcalin și acumulărilor de substanțe reductive (glutation, cisteină, NADH, glucoză), în contrast cu starea de oxidoză pe care o întâlnim în exteriorul celulei menținută prin acidul lactic și protonii exportați în mod sistematic cu ajutorul pompelor exprimate special în acest scop. Ca atare, avem un dezechilibru pH și redox marcant, caracterizat printr-o stare intracelulară de alcaloză și redoză și printr-o stare extracelulară de acidoză și oxidoză . Neînțelegerea acestui mecanism face aproape imposibilă o terapie eficientă contra celulelor tumorale.
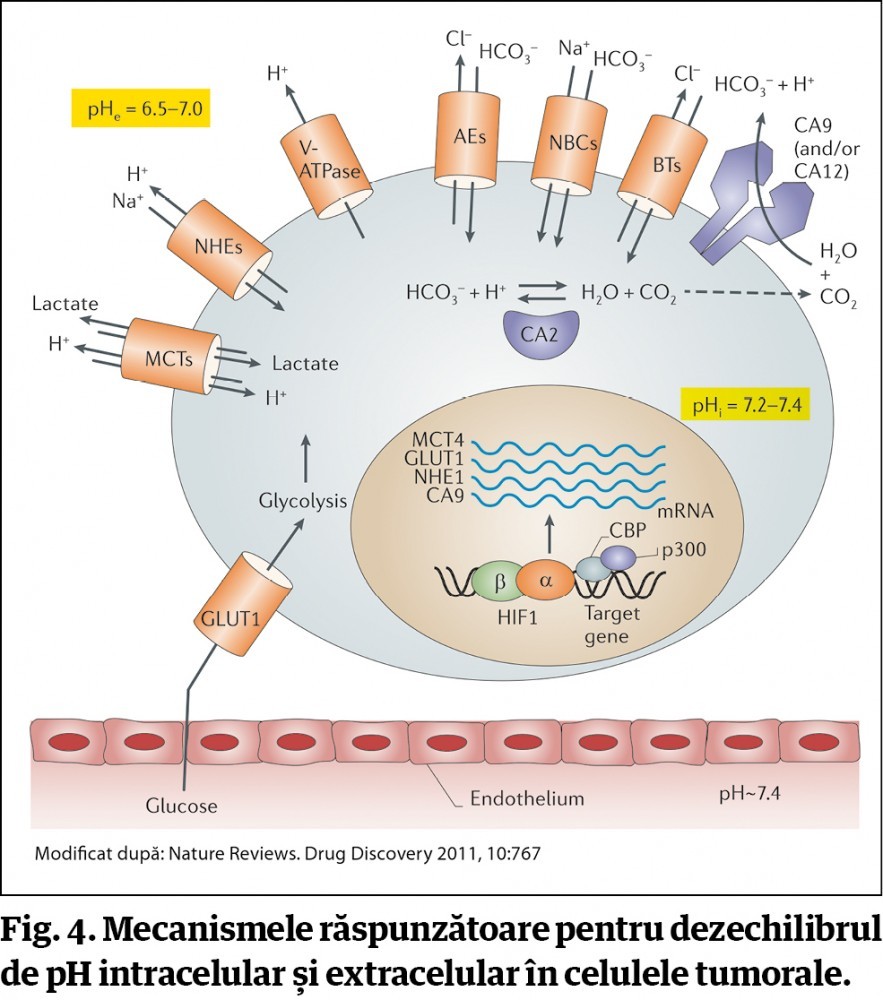
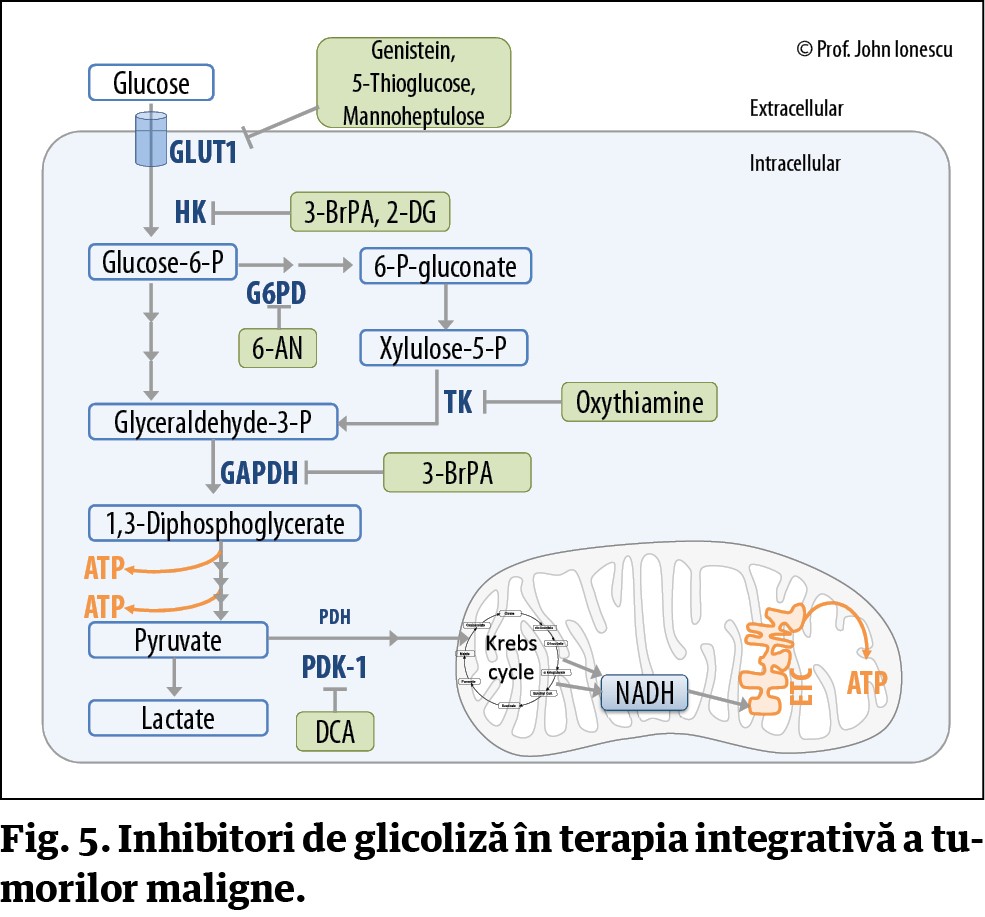
Al doilea marker crucial, metabolic al celulelor tumorale este glicoliza aerobă, așa-numitul efect Warburg, descoperită de savantul german Otto Warburg în anul 1929. Glicoliza aerobă conferă un alt avantaj enorm, de supraviețuire, celulelor tumorale. În biologie și medicină este cunoscută în primul rând glicoliza anaerobă, caracteristică anumitor microorganisme, dar și celulelor diferențiate la mamifere, care intervine în situația lipsei de oxigen – aceasta înseamnă fermentarea glucozei în lipsa oxigenului. Celula malignă folosește această glicoliză nu numai în absența oxigenului, cum întâlnim în special în tumorile primare hipoxice, prost vascularizate, dar și în prezența oxigenului (de unde și denumirea de glicoliză aerobă), ceea ce face necesar un consum imens de glucoză, de 14-20 de ori mai mare decât în cazul celulelor normale, realizat prin cuplarea glicolizei cu shunt-ul pentozofosfatic. Consumul de glucoză, dar și de fructoză este necesar metabolismului glicolitic al celulelor maligne și producerii de ATP necesar sintezelor și multiplicărilor celulare. Ca atare, celula malignă își creează un echipament special, cu așa-numiții transportori de glucoză la nivel de membrană (GLUT1-4), epuizând toate rezervele glucidice ale organismului în scopul propriei multiplicări și expansiuni. De aceea, pentru terapie este foarte important să se înțeleagă rolul dezechilibrului acido-bazic menționat anterior și al acestui mecanism de glicoliză aerobă caracteristic celulelor tumorale.
La fel de important este faptul că în momentul reducerii aportului de glucoză imperios necesar creșterii tumorii, aceasta va schimba substratul energetic, importând în mod masiv acidul glutamic rezultat din activarea procesului de glutaminoliză.
Pentru terapeut este relevantă și observația că celulele tumorale nu pot metaboliza grăsimile și nu pot, prin urmare, crește și prolifera în momentul în care organismul primește o dietă ketogenică, care favorizează tocmai obținerea energiei prin metabolizarea corpilor cetonici (aceto-acetat, beta hidroxibutirat, acetonă) rezultați din oxidarea grăsimilor. Pe baza acestor caracteristici metabolice este evident că terapeutul nu poate recomanda o hrană bogată în carbohidrați cu indice glicemic crescut, cum ar fi zaharurile, făinoasele, fructele și băuturile dulci și consumul de alcool. De aceea, terapeutul trebuie să aleagă cu atenție atât lipidele necesare metabolismului energetic, cât și proteinele, respectiv aminoacizii necesari menținerii masei musculare, care să nu favorizeze la rândul lor creșterea tumorală.
ZDS: Ce ne puteți spune despre apariția metastazelor, din ce cauze se produc și cum apar? Au același tratament ca și boala primară?
Prof. John Ionescu: Metastazele apar prin migrarea pe cale sangvină sau limfatică a celulelor din tumora primară și instalarea lor în alte țesuturi sau organe. Această răspândire a celulelor tumorale este posibilă, în primul rând, prin mediul acid creat de tumoră în jurul ei, prin eliminarea continuă de acid lactic. Starea de acidoză extracelulară astfel generată permite expansiunea tumorală rapidă în țesuturile înconjurătoare și ca atare trebuie combătută terapeutic. Tratamentul metastazelor poate fi privit în mod diferențiat, așa cum explicăm în cadrul cursului din data de 19 martie a.c., întrucât aceste formațiuni tumorale au în mod preponderent un metabolism aerob, deosebit de metabolismul anaerob al tumorii primare, și o heterogenicitate genetică mai accentuată decât tumora primară. În plus, ele reacționează deosebit de sensibil la stimulanții beta-adrenergici descărcați în situațiile de stres și care activează puternic oncogene prometastatice.
ZDS: Ce se înțelege în medicina integrativă prin tratament personalizat al pacienților cu cancer?
Prof. John Ionescu: Răspunsul la această întrebare îl oferim detaliat la Cursul de Medicină Integrativă din data de 19 martie a.c. În cadrul cursului documentăm deosebirile metabolice între o tumoră cu creștere rapidă, bazată pe o glicoliză aerobă fulminantă, care necesită un consum de glucoză imens, și formele mai lente de evoluție tumorală, în care poate predomina consumul de aminoacizi, în special de glutamină și respectiv acid glutamic, prin procesul de glutaminoliză. De asemenea, mai există și formele finale ale unei maladii canceroase marcate printr-o cașexie acută, cu consum de masă musculară, de albumină serică, care și ele fac necesară o intervenție personalizată. Ca atare, terapeutul trebuie mai întâi să identifice ce fel de metabolism energetic caracterizează tumora în momentul primei întâlniri cu pacientul, pentru a alege cele mai bune elemente terapeutice de compensare atât a echilibrului acido-bazic și redox, cât și în blocarea formelor esențiale de metabolism energetic, referindu-mă aici la glicoliza aerobă și la shuntul pentozofosfatului pe de o parte, la glutaminoliză sau la metabolismul grăsimilor, pe de altă parte. De aceea, investigarea markerilor tumorali caracteristici proceselor energetice, metabolice și de dezintoxicare menționate anterior este esențială pentru alegerea conduitei terapeutice. În orice caz, scopul final al unei terapii integrative este și rămâne acela de a dăuna în mod specific celulelor tumorale, fără a afecta celulele normale din organismul uman.
În acest sens, evaluarea enzimelor sau produșilor de metabolism energetic caracteristice unei faze metabolice sau alteia (piruvat/lactat, TKTL1, M2PK, echilibrul acido-bazic și redox, prezența cașexiei) poate conduce la o serie de decizii terapeutice corespunzătoare, pe care le prezentăm la curs.
ZDS: Care considerați că sunt cele mai importante lucruri de știut pentru un medic care tratează cancerul?
Prof. John Ionescu:
- Medicul oncolog modern trebuie să aibă permanent în vedere că:
- Factorii care au indus tumora se află chiar în interiorul tumorii (organotoxine, metale tranziționale, virusuri).
- Biochimia celulei tumorale este deosebită de biochimia celulei sănătoase din țesutul înconjurător și conferă avantaje excepționale celulei tumorale în capacitatea de a supraviețui, de a se multiplica și de a metastaza.
- Metabolismul energetic al celulei tumorale care favorizează această creștere poate fi susținut în necunoștință de cauză printr-o alimentație nerațională, bogată în alimente cu indice glicemic crescut (dulciuri, făinoase, fructe, sucuri dulci), în substanțe reducătoare (de genul glutationului, NADH, cisteinei și glucozei, în primul rând).
- Antioxidanții sau alte elemente fiziologice, precum zincul, glutationul, vitamina E sau anumiți aminoacizi, de genul glutaminei/glutamatului, serinei, glicocolului, metioninei, pot favoriza creșterea neoplazică și ca atare trebuie pe cât posibil îndepărtați din hrana zilnică.
Există o serie întreagă de posibilități de a inhiba creșterea tumorală prin alte elemente naturale pe care le prezentăm la curs, printre ele vitamina C, polifenolii, inhibitorii de glicoliză, dieta ketogenică ș.a.
ZDS: Ce ne puteți spune despre implicarea sistemului imunitar în terapia anticancer? Mulți specialiști nu recunosc că sistemul imunitar ar avea vreo implicare în aceste maladii.
Prof. John Ionescu: Ceea ce cunoaștem cu toții este așa-numita paralizie imunitară în boala canceroasă. Una dintre cauzele principale este suprimarea funcțiilor celulelor imunitare, de genul macrofagelor și celulelor NK (natural killer), în mediul acid peritumoral amintit anterior (profil imunologic de tip TH2).
Pe lângă inducerea unei paralizii imunitare în mediul acid extracelular, celulele tumorale își maschează antigenele de suprafață într-un glicocalix imens, rezultat dintr-o proliferare enormă a glucidelor și a glicoproteinelor de membrană, nemaiputând fi recunoscute ca non-self de celulele sistemului imun.
ZDS: Dr. Tulio Simoncini considera că principala cauză a tumorilor ar fi ciupercile Candida, dezvoltând o întreagă filosofie și terapie sistemică și locală antifungică (în special prin alcalinizarea organismului). Ce părere aveți de teoria lui Simoncini, are logică și aplicabilitate practică?
Prof. John Ionescu: Ciupercile de genul Candida proliferează ușor în momentul în care apărarea imunitară locală este slăbită. Acest lucru se poate întâmpla la nivel cutanat, pulmonar, intestinal ș.a.m.d. Infecțiile sistemice cu ciupercile de gen Candida sunt extrem de rare. Personal nu cunosc vreun studiu controlat, în care să se fi dovedit prezența ciupercilor Candida în tumorile maligne. Terapia alcalinizantă oferită de dr. Simoncini are însă un efect pozitiv prin neutralizarea mediului acid peritumoral, de care am vorbit anterior și pe care îl identificăm sub forma unei acidoze metabolice. Această neutralizare a mediului acid realizează atât o inhibare semnificativă a capacității de metastazare a tumorilor, cât și o revenire a funcțiilor imunitare ale celulelor din jurul tumorii. Această alcalinizare, pe care o folosim și noi în terapia noastră, are un efect deosebit de pozitiv pentru evoluția tratamentului.
ZDS: Având în vedere modificările extra și intracelulare de pH și potențial redox pentru biologia celulei tumorale, care sunt consecințele în alegerea alimentelor și terapiilor cu efect pro- sau antioxidativ?
Prof. John Ionescu: Este evident din punct de vedere metabolic și terapeutic că nu putem compensa o redoză intracelulară administrând elemente nutriționale cu efect reductiv și antioxidant de genul vitaminei E, zincului, glutationului, zaharurilor. În același timp, datele pe care le avem la dispoziție ne arată necesitatea unei alimentații bogate în vegetale, sucuri de legume cu caracter pro-oxidativ, bogate în acizi organici și polifenoli. La întâlnirea cu metalele din celulele canceroase, polifenolii, ca și vitamina C se autooxidează, producând o explozie de radicali liberi cu efect apoptotic asupra celulelor canceroase. Vitamina C și polifenolii, de genul resveratrolului, quercetinei, curcuminului, administrați intravenos în concentrații farmacologic active, sunt adevărate minuni ale naturii. Administrate pe cale orală în dozele uzuale suplimentele alimentare rareori conduc la un rezultat. Alegerea elementelor nutriționale se poate face în mod științific, măsurând potențialul redox al legumelor și fructelor oferite, putând deosebi astfel între alimente cu un potențial redox pro-oxidativ (de genul sucului de morcov, țelină sau grapefruit) și alimente cu potențial pro-reductiv (de genul sucului de sfeclă roșie sau de pepene, care nu trebuie oferite acestor pacienți din cauza cantității mari de zahăr pe care îl conțin). Alegerea corectă a acestor alimente joacă un rol deosebit în creșterea eficienței terapiei la acești pacienți, hrana corespunzătoare având valoarea celui mai bun medicament.
ZDS: Tratamentele actuale au o eficiență destul de redusă. Cum interferă ele cu energetica celulelor sănătoase, precum și a celor canceroase?
Prof. John Ionescu: Tratamentele actuale țintesc distrugerea celulelor tumorale printr-un mecanism în general pro-oxidativ, mă refer aici atât la radioterapie, cât și la o serie de chemoterapeutice. Majoritatea acestor tratamente nu vizează însă în mod specific metabolismul energetic al celulei canceroase (glicoliza aerobă sau glutaminoliza) și au din păcate numeroase efecte negative asupra țesuturilor și organelor sănătoase din organism, efecte pe care le cunoaștem și le regretăm. Interferențe nefaste apar în momentul asocierii terapiilor antioxidante cu terapiile clasice (chemo și radioterapie) cu efect prooxidativ.
În mod logic, și dovedit experimental, eficiența terapiilor clasice de reducere a tumorilor prin radioterapie și inhibarea angiogenezei scade dramatic în momentul administrării simultane a unor antioxidanți de genul vitaminei E, glutationului, NADH-ului, cisteinei și glucozei. Dimpotrivă, aceste terapii pot fi potențate în mod semnificativ printr-o dietă ketogenică cu potențial prooxidativ, asociată cu inhibitori de glicoliză de genul 2-deoxiglucozei, 3-Br-piruvatului, dicloracetatului, sau a inductorilor de apoptoză prin radicali liberi de genul vitaminei C și a polifenolilor.
Pe parcursul Cursului privind abordarea integrativă a bolii canceroase exemplificăm în mod repetat rolul deosebit de benefic al alimentelor cu potențial pro-oxidativ și demonstrăm efectele negative ale terapiilor antioxidante.
ZDS: Dieta bogată în carbohidrați favorizează redoza celulară, glucoza fiind principalul combustibil al celulei canceroase. Explicați-ne, vă rugăm, semnificația clinică a metabolismului glucidic tumoral și importanța stabilirii unui plan nutrițional!
Prof. John Ionescu: Celulele tumorale beneficiază de mecanisme proprii deosebit de eficiente în captarea glucozei din circulație prin intermediul așa-numiților transportori de glucoză și fructoză (GLUT1-4). Receptorii de insulină sunt și ei într-o cantitate mult mai mare pe suprafața celulelor tumorale decât pe suprafața celulelor normale. Ca atare, orice hrană bogată în carbohidrați, care în tubul digestiv sunt transformați în glucoză, nu face decât să accelereze creșterea și multiplicarea celulelor tumorale, care procesează glucoza și fructoza pe calea glicolizei aerobe și, respectiv, a shunt-ului pentozofosfatului. De aceea, dulciurile de toate felurile, făinoasele și chiar pâinea trebuie privite cu deosebită reținere și înlocuite cu legumele cu un indice glicemic mic, cu anumite amestecuri de aminoacizi pentru menținerea masei musculare și lipide. Acestea din urmă trebuie să conțină acizi grași nesaturați (omega 3 – ulei de in, cânepă sau pește) sau trigliceride cu catenă medie MCT (ulei de cocos). Se înțelege astfel că perfuziile cu glucoză administrate în mod nefericit pacienților oncologici nu fac decât să le scurteze viața.
ZDS: Este dieta ketogenică o soluție pentru echilibrarea metabolică a pacientului cu cancer?
Prof. John Ionescu: În foarte multe cazuri, da, în special când avem de a face cu tipologia marcată printr-o glicoliză aerobă puternic exprimată. În astfel de situații, zaharurile trebuie înlocuite cu o hrană ketogenă completată eventual cu amestecuri speciale de aminoacizi pentru evitarea consumului propriilor proteine musculare sau plasmatice (albumina), caracteristice cașexiei tumorale.
ZDS: Ce înseamnă postul terapeutic și care este rolul acestuia? De ce este importantă asocierea postului terapeutic cu hipertermia (sauna) și sportul în creșterea eficienței metodelor integrative de tratament al cancerului?
Prof. John Ionescu: Postul, așa cum l-a lăsat Dumnezeu, are un rol extraordinar în curățirea organismului, în activarea proceselor de dezintoxicare și în instalarea unei stări pro-oxidative, deosebit de utilă în tratamentul bolii canceroase. Postul, asociat cu un efort fizic aerob, de intensitate medie, accentuează efectul pro-oxidativ anti-tumoral, reducând metastazarea, creșterea tumorală etc. Menționăm că nu este vorba despre un post îndelungat, ci recomandăm un post scurt, intermitent, de 3, maximum 5 zile, asociat cu sucuri de legume cu potențial pro-oxidativ (metoda Gerson). În cadrul cursului exemplificăm tocmai asocierea benefică a radioterapiei cu postul pe termen scurt menționat mai sus.
ZDS: Sunt suplimentele alimentare indicate în terapia integrativa a bolii canceroase? Există și contraindicații?
Prof. John Ionescu: După cum am menționat mai sus, administrarea suplimentelor alimentare cu potențial prooxidativ la nivelul tumorii (curcumină, quercetină, resveratrol, vitamina C, seleniu etc.) în doze farmacologic active constituie un element esențial în terapia integrativă a bolii canceroase.
Pe de altă parte, suplimentarea cu elemente antioxidative și pro-reducătoare de genul glutationului, cisteinei, NADH-ului, zincului, vitaminei E, glutaminei etc. diminuează efectele oricărei terapii prooxidative anticanceroase, favorizând în mod evident creșterea tumorii.
ZDS: În clinica dvs. tratați cancerul? Cum vă pot contacta pacienții români?
Prof. John Ionescu: Clinica din Neukirchen este specializată în tratarea celor mai dificile boli alergice, dermatologice și de mediu. Datorită experienței și rezultatelor obținute în tratamentul tumorilor asociate maladiilor menționate, primim în ultimii ani și un număr din ce în ce mai crescut de pacienți cu boli neoplazice. Acești pacienți, diagnosticați și tratați inițial prin terapiile oncologice curente, caută cu disperare o soluție terapeutică care să le permită regenerarea organismului între ciclurile de chemo- sau radioterapie și evitarea recidivelor. Tratamentul staționar sau ambulatoriu oferit de clinica noastră răspunde acestor cerințe.
Pentru contact: spezialklinik-neukirchen.de,
Tel. +49-9947-28-101.